
腸道僅僅是消化器官嗎? 它其實是人體最長的「免疫邊境線」
我們總以為免疫力藏在血液裡、躲在淋巴結中,卻忽略了身體裡那條長達十米的「隱形防線」——腸道。它不僅是消化器官,更是人體最大、最活躍的免疫器官。近70%的免疫細胞駐紮於此,這不是比喻,而是生物學與醫學證實的健康真相。
今天,就讓我們從演化的底層邏輯出發,探討腸道為何成為這場精密平衡的「和諧戰場」,並如何悄無聲息地決定我們的整體健康。
規模之戰:從皮膚到腸道的防禦擴張
許多人未曾意識,腸道是身體最龐大的免疫中樞。一組直觀的數據對比便能揭示其戰略地位:
- 皮膚,我們的外部屏障,表面積約1.8平方米。
- 腸道黏膜,若將其無數褶皺完全展開,面積可達300至400平方米——相當於兩個標準籃球場。
更關鍵的是,腸道是人體唯一持續與外界相通的內部管道。從口腔到肛門,這條十米長的通道每日迎接食物、微生物等無數外來物質,是身體與外界交互最頻繁的「前沿陣地」。而演化的邏輯從來是:哪裡有挑戰,哪裡就演化出防禦。

演化的雙重壓力:吸收營養 vs. 抵禦入侵
在億萬年的演化歷程中,腸道面臨著持續的「雙重選擇壓力」:它必須從複雜的外界物質中高效吸收營養以維持生存,同時又要時刻抵禦有害微生物(細菌、病毒、寄生蟲)的入侵以避免死亡。
這種壓力,推動腸道演化出一套極其精密且智慧的免疫防禦體系。
- 常備軍與快速反應部隊:
在腸道黏膜的褶皺中,駐紮著海量「免疫尖兵」:樹突狀細胞、巨噬細胞、自然殺傷細胞(NK細胞)等,它們如同24小時不間斷巡邏的邊境哨兵,能快速識別並攻擊入侵者。 - 特異性生化武器:
腸道上皮細胞會分泌大量免疫因子,如免疫球蛋白A(IgA)。這類抗體是演化而來的「特製導彈」,能精準中和病原體,是黏膜免疫的核心武器。 - 物理防線:黏液屏障
腸道持續分泌的黏液層,常被低估,卻是演化的巧妙設計。它不僅潤滑腸道,更如同一張「粘蟲網」,能物理性捕捉有害微生物,防止其直接接觸並穿透腸黏膜上皮細胞。這層「天然防火牆」的完整性,直接決定了免疫防線的第一道強度。
終極智慧:區分「友軍」與「敵人」的平衡藝術
從演化視角看,腸道的終極使命,是平衡兩個看似矛盾的任務:高效吸收 vs. 嚴密防禦。
這要求腸道免疫系統必須具備極高的「識別智慧」。這份智慧,是億萬年理化與生物攻防中錘煉出的捷徑,使其能精準區分:營養物質、有益共生菌(友軍) 與 條件致病菌、明確病原體(敵人)。
這種「既不放過敵人,也不誤傷友軍」的智慧一旦失衡,便解釋了許多生活現象:
- 腸道健康者:往往體魄強健,少受小病困擾。
- 腸道易激者:稍食生冷油膩便腹脹、腹瀉,其本質常是腸黏膜屏障受損、免疫防線出現漏洞,導致無害刺激也被誤判為威脅,引發過度反應。
中醫視角的「脾為後天之本」的現代解碼
當現代免疫學說「腸道是最大免疫器官」,中醫早在兩千年前就提出:「脾為後天之本,氣血生化之源」。所有的營養吸收,免疫防禦的根本都在脾胃,也就是脾胃沒養好,你所吃的高貴營養品都等於白吃了。
- 「脾主運化」腸道具有營養吸收,輸送與黏膜的屏障功能。
- 「脾虛濕盛」實則暗合「腸漏→慢性炎症→代謝紊亂」的現代路徑
- 「脾統血」更與腸道免疫細胞調控全身免疫反應的機制遙相呼應
一旦失衡,如何導致全身性疾病?
當這種精密的平衡被長期打破,後果可能超出消化系統本身,這正是當代醫學的研究前沿:
- 「腸漏」與系統性發炎:屏障損傷使未完全消化的食物顆粒或細菌產物進入血液,可能引發全身性、低度慢性發炎,被認為與自體免疫疾病(如:類風濕關節炎,紅斑性狼瘡,多發性硬化症)、過敏、糖尿病、糖化血紅蛋白過高等代謝症候群,甚至與一個人的情緒障礙存在潛在關聯。
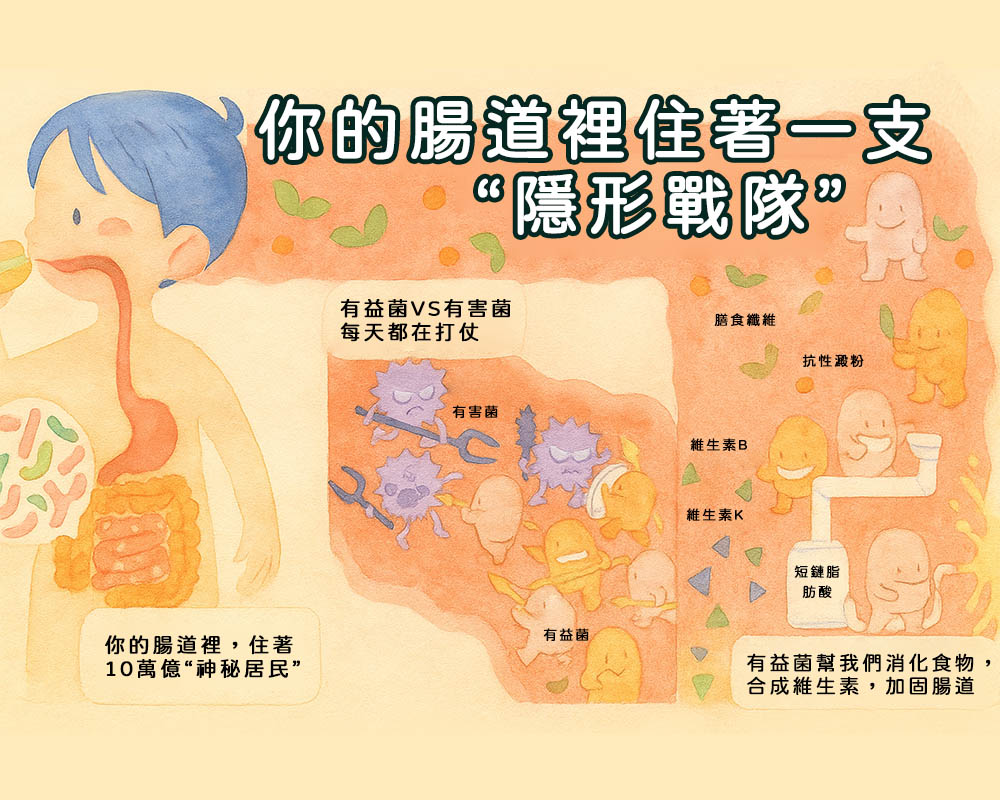
- 共生菌群:不可或缺的免疫教練:一個50公斤的人,腸內菌群重達1.5-2公斤。這些萬億級的「共生夥伴」是演化形成的終極搭檔。它們不僅助消化、合成維生素,更能深度訓練與調節免疫系統:例如,其代謝產生的短鏈脂肪酸(如丁酸),能直接滋養腸上皮細胞、強化屏障,並促進具有抗炎功能的調節性T細胞生成。簡單的說:健康的菌群,是免疫系統的最佳「教練團」。
- 腦腸軸:看不見的熱線:腸道菌群還能通過「腦腸軸」這條雙向通道,藉由神經、內分泌與免疫訊號,直接與大腦溝通,影響壓力反應、情緒甚至認知功能。
結語
因此,腸道健康遠非「消化好」這麼簡單。它是一座由演化精心設計、集物理屏障、細胞大軍、生化武器與微生物盟友於一體的「隱形免疫指揮部」。它的穩定,維繫著營養吸收與免疫防禦的絕妙平衡;它的失衡,則可能成為多種慢性疾病的根源。
呵護腸道,已不僅是為了舒適的消化,更是為全身免疫系統與長期健康,築牢最根本的基石。
參考資料:
- Hooper, L. V., Littman, D. R., & Macpherson, A. J. (2012). Interactions between the microbiota and the immune system. Science, 336(6086), 1268–1273. 這篇《Science》文章指出在無菌小鼠模型中證實,沒有腸道菌群的小鼠免疫系統發育嚴重缺陷。引入特定細菌可誘導免疫細胞(如調節性T細胞)的生成。
- Cryan, J. F., & Dinan, T. G. (2012). Mind-altering microorganisms: the impact of the gut microbiota on brain and behaviour. Nature Reviews Neuroscience, 13(10), 701–712. 腸道免疫狀態可通過迷走神經、細胞激素等途徑影響中樞神經系統,與憂鬱、焦慮、自閉症譜系障礙等有關。探討腸腦軸的經典之作。
- Fasano, A. (2012). Leaky gut and autoimmune diseases. Clinical Reviews in Allergy & Immunology, 42(1), 71–78. 由提出「zonulin」蛋白與腸漏機制的的綜述。
- Arpaia, N., et al. (2013). Metabolites produced by commensal bacteria promote peripheral regulatory T-cell generation. Nature, 504(7480), 451–455. 腸道菌群分解膳食纖維產生的丁酸、丙酸等短鏈脂肪酸,能直接作用於免疫細胞,具有強大的抗發炎效果。本文揭示了丁酸如何促進調節性T細胞的產生。
延伸閱讀:
萬病始於腸道:從中醫「後天之本」到現代「菌叢生態」的健康保衛戰
肺與腸的千年對話:從中醫「肺與大腸相表裡」到現代醫學「肺腸軸」的驚人匯流





